EX-01
Em uma reação de
decomposição de água oxigenada (peróxido de hidrogênio), observou-se a seguinte
variação da massa de água oxigenada em função do tempo:
Calcular a velocidade média
de decomposição da água oxigenada, nessa reação, no intervalo de 2 ~ 4
minutos.
Solução:
Sabemos
que:
Portanto,
EX-02
A cronometragem de uma
reação de saponificação do acetato de etila
revelou os seguintes
resultados:
Calcular as velocidades
médias, dessa reação, em cada um dos intervalos mencionados. O que se pode concluir desses resultados?
Solução:
Para cada intervalo de tempo
vale a relação:
Resumindo temos,
Podemos observar que a
velocidade média diminui com o tempo.
EX-03
Na decomposição de água
oxigenada, em certas condições experimentais, produz-se oxigênio à razão de 1,6
g/min. Calcular a velocidade dessa reação em moles de água oxigenada por hora
(H=1, O=16).
Solução:
Escrevendo a equação de
decomposição:
Resposta: Velocidade da
reação é 6 moles de água oxigenada por hora.
EX-04
Dada a reação química X + Y
→ Z, se duplicarmos, simultaneamente, as concentrações de X e Y e mantivermos todos
os fatores físicos constantes; o que acontece com a velocidade da reação?
Solução:
Sabemos que a velocidade de
uma reação é proporcional às concentrações molares dos reagentes, elevadas a
expoentes iguais aos seus coeficientes na equação química correspondente.
Logo, duplicando a
concentração de X e Y, temos:
EX-05
A reação
está se processando num
recipiente fechado, e em condições tais que sua velocidade obedece a equação
Calcular a variação da
velocidade da reação quando duplicarmos as concentrações molares de nitrogênio
e do hidrogênio e mantendo todas as demais condições constantes.
Solução:
EX-06 === RESUMO ===
1) Cinética química estuda a
velocidade das reações químicas;
2) Velocidade
média de uma reação química é o quociente entre a variação do número de moles
de um dos participantes da reação pela variação do tempo; em geral, a
velocidade é definida para os reagentes e, por isso, representada pela fórmula:
3) Velocidade instantânea é
o limite da velocidade, quando o intervalo de tempo tende à zero;
4) A velocidade das reações
pode ser medida por processos químicos e físicos, sendo preferíveis os físicos;
5) No estudo da velocidade
das reações destacam-se as teorias das colisões e do complexo ativado;
6) Tudo indica que o número de choques é
fundamental na determinação da velocidade de uma reação; então, torna-se
importante levar em conta as seguintes características dos “choques”:
Freqüência dos choques, energia (violência) dos choques e orientação apropriada das moléculas no
instante do choque;
7) O estado particular dos
reagentes inclui muito na velocidade das reações; neste particular devemos
levar em conta: estado físico, estado nascente dos gases, estado cristalino dos
sólidos e o fato de estar ou não em solução, pois tudo isto influi na
subdivisão das partículas reagentes, facilitando ou dificultando o contato
entre as mesmas;
8) Um aumento de temperatura
sempre provoca um aumento na freqüência dos choques e na energia (violência)
dos choques entre as moléculas, acarretando sempre um aumento na velocidade das
reações. Em geral o aumento de
temperatura aumenta a velocidade das reações endotérmicas e das reações
exotérmicas;
9) Energia de ativação é a
energia necessária para as moléculas atingirem o estado ativado, onde se forma
o complexo ativado;
10) Além do calor, outras
formas de energia que podem influir na velocidade das reações são a eletricidade
e a luz;
11)
Aumentando a concentração dos reagentes iremos aumentar a freqüência dos
choques entre as moléculas e, consequentemente, a velocidade da reação irá
aumentar. Este fato é traduzido pela fórmula geral:
que representa a Lei da ação
das massas ou Lei de Guldberg-Waage
12) Quando uma reação ocorre
em várias etapas, a velocidade global dependerá da etapa mais lenta, que é
denominada etapa determinante da velocidade da reação;
13) Um catalisador aumenta a velocidade da
reação e não é consumido; um inibidor diminui a velocidade da reação e é
consumido;
14) Os principais mecanismos da catálise são:
a) Formação de um composto intermediário;
b) Adsorção dos reagentes (adsorção = processo pelo qual átomos, moléculas ou íons são retidos (fixados) na superfície de sólidos através de interações de natureza química ou física);
15) Os principais
catalisadores são: metais, óxidos metálicos, ácidos, bases, substâncias que se
oxidam e reduzem facilmente.
EX-07 (Mauá)
A concentração [A], expressa
em mol/ℓ de uma substância A que, em meio homogêneo, reage com outra B, segundo
a equação A + B à C + D, varia com o tempo t segundo a
lei: [A] = 5 – 0,2t – 0,1t², com t medido em horas. Qual a velocidade média dessa reação entre os
instantes t1 = 1h e t2 = 2h?
Solução:
Resposta: vm =
0,5 mol/ℓ.h
EX-08
Em determinada experiência,
a reação de formação de água está ocorrendo com o consumo de 4 mols de oxigênio
por minuto. Qual é a velocidade de consumo de hidrogênio?
Solução:
EX-09 (UnB)
Assinale as opções corretas:
01. O catalisador afeta a velocidade de uma reação porque aumenta o número de moléculas com energia cinética maior ou igual à energia de ativação da reação.
01. O catalisador afeta a velocidade de uma reação porque aumenta o número de moléculas com energia cinética maior ou igual à energia de ativação da reação.
04. A concentração dos
reagentes afeta a velocidade de uma reação porque há alteração no número de
colisões efetivas.
08. Uma reação ocorre
quando há colisão efetiva entre as moléculas reagentes, numa orientação
apropriada.
EX-10 (UF Ouro Preto – 2010)
O óxido nítrico é um
poluente atmosférico que pode ser reduzido na presença de hidrogênio, conforme
a seguinte equação:
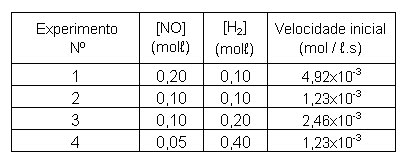
A velocidade inicial de
formação de N2 foi medida para várias concentrações iniciais
diferentes de NO e H2, e os resultados são os seguintes:
Fazendo uso desses dados,
determine:
a) a equação de velocidade
para a reação;
b) o valor da constante de velocidade da reação;
c) a velocidade inicial da reação quando [NO]= 0,5 mol/ℓ e [H2]= 1,0 mol/ℓ.
b) o valor da constante de velocidade da reação;
c) a velocidade inicial da reação quando [NO]= 0,5 mol/ℓ e [H2]= 1,0 mol/ℓ.
Solução:
a)
Analisando a tabela
observa-se que da experiência 2 para a experiência 1 a concentração de NO ([NO])
dobra, a concentração de H2 [H2] é constante e a velocidade da reação quadruplica, isto
significa que: [NO]² .
Novamente, na tabela,
observa-se que da experiência 2 para a experiência 3 a concentração de H2 ([H2])
dobra, a concentração de NO ([NO]) é constante e a velocidade da reação também
dobra, isto significa que: [H2]1.
Logo: Podemos concluir que a equação de velocidade
da reação é:
b)
Utilizando os dados da
experiência 1:
c)
[NO]= 0,5 mol/ℓ e [H2]=
1,0 mol/ℓ.





















Nenhum comentário:
Postar um comentário